
纳米抗体(Nanobody)由于其结构简单、稳定性高以及易于工程化改造,近年来在抗体工程和生物医药研究中受到了广泛关注。与传统抗体相比,纳米抗体仅由驼科重链抗体的可变区(VHH)构成,分子量通常只有约15 kDa。这种单域结构不仅赋予纳米抗体更好的溶解性和稳定性,也使其更容易通过基因工程进行模块化设计。然而,单个纳米抗体在某些应用中仍然存在局限,例如结合能力有限、功能单一以及在复杂生物系统中难以产生足够强的生物学效应。因此,近年来研究重点逐渐转向纳米抗体的多聚化(multimerization)和多特异性(multispecificity)工程设计,通过组合多个纳米抗体模块来提升其功能性能。
纳米抗体多价化的核心思想是利用多个抗体结构域协同作用,从而增强整体结合能力和生物学功能。当多个纳米抗体同时作用于同一靶标时,会产生明显的“亲合力效应(avidity principle)”,使抗体整体亲合力显著高于单个结合位点。这种效应在抗病毒抗体、肿瘤靶向抗体以及受体调控研究中尤为重要。例如,在病毒中和研究中,多价纳米抗体可以同时结合病毒表面的多个表位,从而显著提高中和能力。在肿瘤免疫治疗领域,多价纳米抗体还可以通过诱导受体聚集来调控细胞信号通路,从而增强治疗效果。正因如此,如何高效构建多价纳米抗体成为抗体工程研究的重要方向。
目前纳米抗体多价化的技术路线大致可以分为两大类:体内组装策略(in vivo assembly)和体外工程化构建策略(in vitro engineering)。体内组装策略主要依赖细胞表达系统,通过基因工程设计,使多个纳米抗体在表达过程中自动形成稳定的多聚结构。这种策略的优势在于表达过程简单、结构均一性较高,并且适合大规模生产,因此在纳米抗体药物开发中得到了广泛应用。
最直接的纳米抗体多价化方法是通过柔性连接肽(linker)将多个VHH结构域在基因水平串联。在这种设计中,多个纳米抗体序列被克隆到同一表达载体中,并通过短肽序列连接形成单一多结构域蛋白。在表达系统中翻译后,该蛋白即形成多价纳米抗体结构。
最常用的linker是富含甘氨酸和丝氨酸残基的柔性肽序列,例如经典的(G4S)n linker。这种linker具有较高柔性,可以减少不同结构域之间的空间干扰,使每个纳米抗体结构域能够独立折叠并保持其抗原结合能力。通过调节linker的长度,可以在一定程度上控制纳米抗体结构域之间的空间距离,从而优化多价结合效果。
除了常用的柔性linker外,弹性蛋白样多肽(ELP)结构域也可作为结构支架,用于组织多个纳米抗体形成更复杂的多价结构。ELP通常由重复的五肽序列(VPGXG)n构成,具有良好的可塑性和结构稳定性,为纳米抗体多价化提供了一种更加灵活的结构框架。
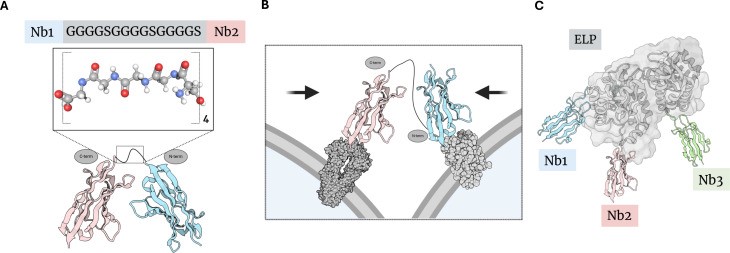
图1 柔性linker串联表达
(A)在纳米抗体Nb1和Nb2之间引入(Gly4Ser)3柔性linker,构建形成一个双价纳米抗体结构。
(B)通过(Gly4Ser)3 linker将两个不同的纳米抗体进行连接,构建形成双特异性纳米抗体结构。这种结构可以形成类似“分子夹钳(molecular clamp)”的构象,使表达相应抗原的两个细胞在空间上更加接近。
(C)ELP结构域可以用于容纳并连接三个不同的纳米抗体结构域,构建三特异性纳米抗体结构。
在抗病毒研究中,研究者通过linker将多个识别同一病毒表位的纳米抗体连接,形成多价结构,从而显著增强病毒中和活性。在肿瘤靶向应用中,也可以将识别不同肿瘤抗原或受体的VHH结构域串联,实现多位点结合或受体聚集,从而增强信号阻断或细胞定向效应。类似策略还被探索用于多特异性免疫调控,例如同时靶向肿瘤抗原和免疫检查点受体,以提高治疗选择性和效力。
另一种非常重要的体内多聚化策略是Fc融合表达(VHH-Fc fusion)。在这种设计中,纳米抗体的C端与IgG抗体的Fc结构域进行基因融合。由于Fc结构域天然能够形成稳定的二聚体结构,因此在表达过程中,两个VHH-Fc融合蛋白会通过Fc区域自发形成二聚体,从而实现纳米抗体的二价化。
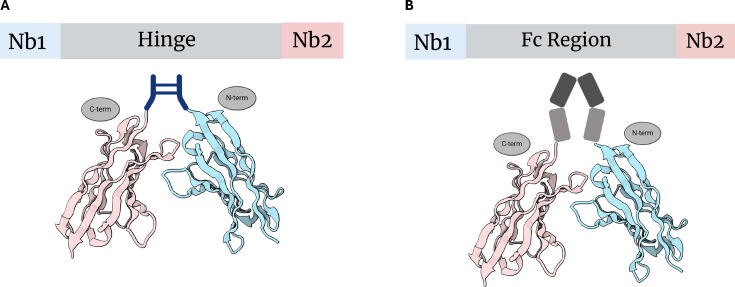
图2 Fc融合表达
(A)在纳米抗体Nb1与Nb2之间引入铰链(hinge)区序列,从而构建形成双价(bivalent)的多聚纳米抗体(polybody)结构。
(B)在纳米抗体Nb1与Nb2之间引入Fc区(crystallizable Fc region)序列,同样构建出双价(bivalent)多聚纳米抗体结构。
这种设计不仅能够增加纳米抗体的结合价数,还可以显著改善其药代动力学特性。传统单域纳米抗体由于分子量较小,在体内往往会被快速肾脏清除,而Fc融合可以增加分子量,并通过与FcRn受体结合延长循环半衰期。此外,Fc结构域还能够介导多种免疫效应功能,例如抗体依赖性细胞毒作用(ADCC)和补体依赖性细胞毒作用(CDC),从而在免疫治疗中发挥更强的生物学效应。因此,VHH-Fc融合蛋白已经成为当前纳米抗体药物开发中最常见的分子形式之一,在肿瘤治疗和抗病毒抗体开发中均有广泛应用。
除了linker串联和Fc融合之外,研究人员还利用多种自组装卷曲螺旋肽(self‑assembling coiled coils and peptides)序列来驱动纳米抗体的多聚化。这些结构域能够在表达过程中通过特定蛋白—蛋白相互作用自发形成稳定的寡聚体,从而将多个纳米抗体模块组装在一起,实现多价或多特异性构建。
例如来自Staphylothermus marinus的右手卷曲螺旋(RHCC)能够形成四聚体结构,将纳米抗体融合到RHCC后可自发生成四价复合物,从而增强整体结合力。类似策略也包括COMPcc,一种由软骨寡聚基质糖蛋白衍生的五链卷曲螺旋结构域,其融合纳米抗体后可形成五价复合物。
此外,这类自组装策略不仅可以在细胞内表达时自发形成,还可以与SpyTag–SpyCatcher系统等模块化共价连接方法结合,在体外精确组装不同数量的纳米抗体模块。利用这种策略,可以将多个纳米抗体模块按需拼接,构建多价或多特异性纳米抗体结构,在不影响单个抗体抗原识别能力的前提下显著增强多价结合效应和功能活性。
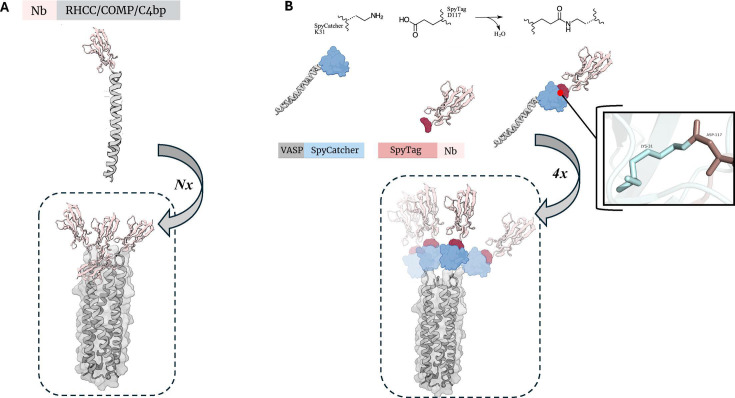
图3 自组装卷曲螺旋肽接导的多聚化
(A)编码自组装coiled-coil结构域的序列被连接到Nb编码序列上。所得的Nb-coiled-coil融合蛋白能够与其他相同的融合蛋白自组装。
(B)利用SpyTag-SpyCatcher系统,将Nb与血管扩张刺激磷蛋白(VASP)进行连接,从而形成一种四聚体结构。
除了利用卷曲螺旋结构域形成有限数目的寡聚体外,研究人员还开发了利用天然蛋白纳米颗粒(protein nanoparticles)作为支架来展示多个纳米抗体结构域的策略。这类方法通常依赖能够自发组装成高阶对称结构的蛋白质,例如细菌毒素亚基、铁蛋白或其他多亚基酶复合体。通过将纳米抗体与这些蛋白亚基进行基因融合,可以在表达过程中形成高度有序的多价抗体结构。
与依赖基因表达系统的体内组装策略不同,体外工程化方法通过酶促或化学介导在蛋白翻译后阶段实现纳米抗体的定向连接。这类策略具有高度灵活性,可以在不同纳米抗体模块之间实现可控拼接,并允许在保持各结构域功能完整的情况下构建复杂的多特异性结构。
一种常见的酶促方法是利用Sortase A转肽酶进行定点连接。Sortase A能够识别特定的LPXTG序列,并在该位点形成酰基中间体,随后通过甘氨酸残基的亲核攻击完成蛋白之间的共价连接。通过在纳米抗体分子末端引入Sortase识别序列,可以实现两个或多个纳米抗体之间的精确定向连接,从而构建双价或多价结构。这种方法具有较高的位点特异性,因此能够避免随机化学偶联带来的结构异质性问题。
除了酶促连接外,化学介导方法也被广泛应用于纳米抗体多聚化。例如,异型双功能交联剂Sulfo-SMCC可以同时与蛋白的氨基和巯基反应,从而形成稳定的硫醚键。通过在纳米抗体上引入特定的反应基团,可以实现不同纳米抗体之间的定向交联。虽然化学介导方法在结构控制方面不如酶促精确,但其操作简单、适用范围广,因此仍然是实验室和工业生产中常用的技术路线。
除了传统的共价连接方法,研究人员还提出了一种利用膜蛋白聚集特性的纳米抗体组装策略。这种方法通过在纳米抗体C端引入单跨膜结构域,使其在表达过程中定位于脂质膜环境中。由于跨膜结构域具有明显的疏水性,这些融合蛋白会倾向于互相聚集,将其跨膜区域隐藏于疏水环境(如膜或膜模拟剂)中,从而促进纳米抗体之间的空间靠近。
为了在体外维持这种结构稳定性,研究人员利用一种称为peptidisc的膜模拟体系对跨膜结构域进行包裹。Peptidisc是一种两亲性多肽结构,其内部疏水区域可以稳定跨膜片段,而外部亲水区域则保证整体复合物在水溶液中的溶解性。通过这种方式,可以形成包含多个纳米抗体的多价复合物。
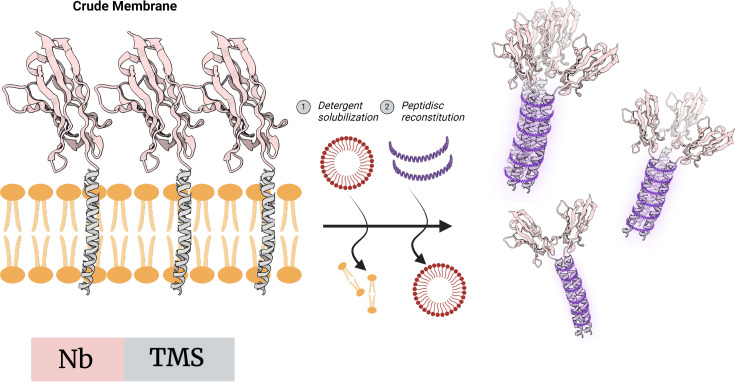
图4 TMS–Nb嵌合体在膜模拟体系中聚集
实验结果表明,这种膜模拟驱动的纳米抗体聚集结构能够显著提高抗原结合能力。例如,在抗GFP纳米抗体系统中,多价聚集结构表现出明显的亲合力增强效应。此外,在ELISA检测体系中,这种多价纳米抗体复合物还能够显著提高检测灵敏度,最高可提升30倍以上。尽管该方法在价数控制方面仍存在一定挑战,但其通过物理聚集驱动多价化的设计思路,为纳米抗体工程提供了一种新的技术方向。
随着多价和多特异性纳米抗体工程技术的不断发展,这类分子在多个生物医药领域展现出广阔的应用潜力。首先,在抗病毒研究中,多价纳米抗体能够同时结合病毒表面的多个表位,从而显著提高中和效率,并降低病毒逃逸突变带来的风险。其次,在肿瘤免疫治疗领域,多特异性纳米抗体可以同时靶向肿瘤抗原和免疫细胞受体,从而实现类似双特异性抗体或T细胞连接器的功能。此外,在诊断和生物分析领域,多价纳米抗体还可以提高检测灵敏度。例如,在免疫检测或生物传感器系统中,通过提高抗体价数可以增强抗原捕获能力,从而显著降低检测限。这一特点使纳米抗体多价化技术在病毒检测、肿瘤标志物检测以及环境监测等领域具有重要价值。
总体而言,纳米抗体多价化与多特异性工程已经成为抗体工程领域的重要研究方向。通过结合体内表达系统、自组装蛋白结构以及体外酶促连接等多种技术路线,研究人员能够根据不同应用需求构建结构多样、功能丰富的纳米抗体分子。这些技术不仅推动了新一代抗体药物的开发,也为诊断试剂和生物分析工具的设计提供了新的思路。
参考文献
Al-Seragi M, Chen Y, Duong van Hoa F. Advances in nanobody multimerization and multispecificity: from in vivo assembly to in vitro production. Biochem Soc Trans. 2025 Feb 7;53(1):235–48. doi: 10.1042/BST20241419.

南京德泰生物工程有限公司 Nanjing Detai Bioengineering Co.,Ltd. ©2026 All Rights Reserved