免疫共沉淀实验流程及注意事项
相关服务:免疫共沉淀检测(CO-IP)
免疫共沉淀(Co-Immunoprecipitation)是以抗体和抗原之间的专一性作用为基础的用于研究蛋白质相互作用的经典方法。是确定两种蛋白质在完整细胞内生理性相互作用的有效方法。 免疫共沉淀实验的操作步骤比较多,要得到一个完美的实验结果,不仅需要高质量的抗体,对免疫沉淀体系也需要有严格的控制指标。在免疫共沉淀的实验过程中,从蛋白样品处理、抗体-琼脂糖珠复合物洗涤到最后的鉴定,每步都非常关键,需要严格控制实验流程中每个关键步骤的质量,才能达到最终的实验目的。
免疫共沉淀实验流程
该免疫共沉淀操作步骤是将抗体先结合到蛋白A/G琼脂糖珠上,然后再与抗原混合。相对其他方法,最终的得率较低,但避免了抗体共洗脱的问题。如果希望获得高纯度的目的蛋白,而不考虑非特异性结合,可以将抗体和蛋白样品在加入蛋白A/G琼脂糖珠之前进行混合,这样最后抗体也会和目的蛋白一同被洗脱下来,从而可能会对蛋白质印迹法(western blot)检测造成干扰。
操作步骤
- 用预冷的磷酸缓冲液洗涤细胞两次,最后一次吸干磷酸缓冲液;
- 加入预冷的RIPA Buffer(1 ml/107个细胞、10 cm培养皿或150 cm2培养瓶,0.5 ml/5×106个细胞、6cm培养皿、75cm2培养瓶);
- 用预冷的细胞刮子将细胞从培养皿或培养瓶上刮离,把悬液转移到干净的1.5ml EP管中。并置于低速摇床,4℃缓慢晃动15min(EP管插冰上,置水平摇床上);
- 4℃,14000rpm离心15min,立即将上清转移到一个新的离心管中;
- 将Protein A/G琼脂糖珠用磷酸缓冲盐溶液洗两遍,用磷酸缓冲盐溶液配制成50%的Protein A/G琼脂糖珠工作液,建议减掉枪尖部分,避免在涉及琼脂糖珠的操作中破坏琼脂糖珠;
- 在样品中以每1ml中加100μl的比例,加入50%的Protein A/G琼脂糖珠工作液。水平摇床4℃摇动10min(EP管插冰上,置水平摇床上),该步骤的目的是去除非特异性结合的蛋白;
- 4℃,14000rpm离心15min,将上清转移到一个新的离心管中,去除Protein A/G琼脂糖珠;
- 做蛋白标准曲线(Bradford 法),测定蛋白浓度,测前将总蛋白至少稀释1:10倍以上,以减少细胞裂解液中去垢剂的影响(定量,分装后,可以在-20℃保存一个月);
- 用磷酸缓冲液将总蛋白稀释到1μg/μl以降低裂解液中去垢剂的浓度。如果觉得你的目的蛋白的浓度低了,可以将总蛋白浓度提高到10μg/μl(假设浓度足够);
- 加入一定体积的抗体到500μl总蛋白中,抗体的稀释比例因与它有作用的蛋白在不同细胞系中的多少而异;
- 4℃缓慢摇动抗原抗体混合物过夜或室温2h;激酶或磷酸酯酶活性分析建议用2h室温孵育;
- 加入100μl Protein A琼脂糖珠来捕捉抗原抗体复合物,4℃缓慢摇动抗原抗体混合物过夜或室温1h,如果所用抗体为鼠抗或鸡抗,建议加2μl过渡抗体;
- 14000rpm瞬时离心5s,收集沉淀,并且用预冷的洗涤缓冲液(或者预冷的磷酸缓冲盐溶液)洗涤3遍(每次加入800μl),RIPA Buffer有时候会破坏琼脂糖珠-抗原抗体复合物内部的结合,可以使用磷酸缓冲盐溶液;
- 用60μl 2×上样缓冲液将琼脂糖珠-抗原抗体复合物悬起,轻轻混匀,缓冲液的量依据上样多少的需要而定(60 μl足够上三道);
- 以游离抗原,抗体,珠子,离心,将上清电泳,收集剩余琼脂糖珠,上清也可以暂时冻-20℃,留待以后电泳,电泳前应再次煮5min变性;
注:RIPA配制:150mM Nacl,1%乙基苯基聚乙二醇,1%脱氧胆酸钠,25mM Tris-HCl缓冲液(PH7.6),0.1%SDS。
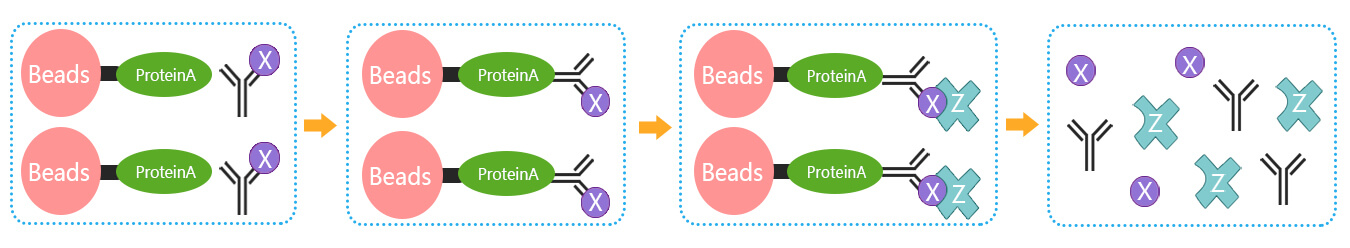
免疫共沉淀实验流程
通过免疫共沉淀确定未知结合蛋白
该实验的思路为:先通过免疫共沉淀实验,得到结合蛋白,随后对得到的结合蛋白进行测序。
- 用磷酸盐缓冲液洗30块10 cm培养板上的适宜细胞。刮去每块板上的细胞到1 ml冰冷的EBC裂解缓冲液中;
- 将每毫升细胞悬液转移到微量离心管中,在微量离心机上4℃以最大速度离心15min;
- 收集上清(约30 ml)并加入30 μg的适当抗体,4℃摇动免疫沉淀物1 h;
- 加入0.9 ml的琼脂糖蛋白A悬液,4℃摇动免疫沉淀物30 min;
- 用含900 mmol/L NaCl的NETN洗琼脂糖蛋白A混合物,再重复洗5次。最后,用NETN洗一次;
- 吸出混合物的液体部分。加入800 μl的1×SDS胶加样缓冲液到球珠中,煮沸4min;
- 将样品加入到大孔的不连续SDS-PAGE梯度胶中,在10mA的恒定电流下电泳过夜;
- 通过考马斯亮蓝染色观察蛋白质泳带;
- 从胶上切下目标带,将其放到微量离心管中,用1ml 50%乙腈洗两次,每次3 min;
- 用胰蛋白酶消化胶中的蛋白质,再进行电洗脱;
- 通过窄孔高效液相色谱分离肽。将收集的肽进行Edman降解测序。
注意事项
1)细胞裂解采用温和的裂解条件,不能破坏细胞内存在的所有蛋白质-蛋白质相互作用,多采用非离子变性剂(NP-40 或Triton- X-100)。每种细胞的裂解条件是不一样的,通过经验确定;
2)不能用高浓度的变性剂(0.2%SDS),细胞裂解液中要加各种酶抑制剂;
3)使用对照抗体:单克隆抗体:正常小鼠的IgG或另一类单抗;兔多克隆抗体:正常兔IgG;
4)确保共沉淀的蛋白是由所加入的抗体沉淀得到的,而并非外源非特异蛋白,单克隆抗体的使用有助于避免污染的发生;
5)要确保抗体的特异性,即在不表达抗原的细胞溶解物中添加抗体后不会引起共沉淀;
6)确定蛋白间的相互作用是发生在细胞中,而不是由于细胞的溶解才发生的,这需要进行蛋白质的定位来确定。
相关服务
相关阅读
免疫共沉淀实验概述
免疫共沉淀实验常见问题解析


